Varón de 90 años que ingresa en planta de Cardiología por descompensación de insuficiencia cardiaca..
Antecedentes personales
Se trata de un varón de 90 años, sin alergias medicamentosas conocidas, ni hábitos tóxicos; con antecedentes de hipertensión arterial en tratamiento con tres fármacos, diabetes mellitus tipo 2 en tratamiento con antidiabéticos orales y dislipemia. Independiente para actividades básicas de la vida diaria. Movilidad limitada por patología articular, deambula con bastón.
Desde el punto de vista cardiológico se encuentra en seguimiento en consultas externas por fibrilación auricular permanente y valvulopatía aórtica degenerativa con estenosis de grado moderado (hipertrofia ventricular izquierda concéntrica moderada y FEVI 68%) al momento del diagnóstico en Julio 2018.
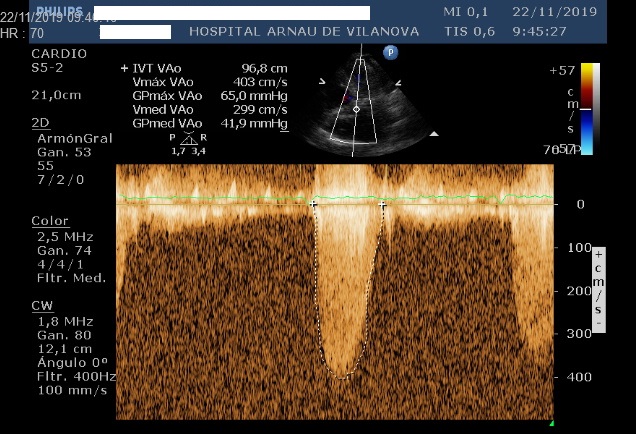
Durante el seguimiento presentó una descompensación leve de insuficiencia cardiaca que se manejó de forma ambulatoria. En la ecografía cardiaca transtorácica de control se evidenció doble lesión aórtica degenerativa con estenosis de grado severo (gradiente medio 40 mmHg, máximo 61 mmHg, relación ITV TSVI/VAo 0,22 y área valvular por continuidad 0,9 cm2) e insuficiencia ligera; con hipertrofia moderada concéntrica del VI y FEVI normal. Durante el seguimiento ambulatorio se objetivó empeoramiento de la clase funcional, por lo que se le plantea tratamiento percutáneo-TAVI.
Enfermedad actual
Acude al servicio de Urgencias de nuestro centro por empeoramiento de la clase funcional en las últimas dos semanas y ortopnea. Refiere aumento de peso y aparición de edemas en extremidades inferiores. Niega dolor torácico ni síncope.
Exploración física
Consciente y orientado en las tres esferas. Bien perfundido globalmente. TA: 138/64 mmHg. Auscultación cardiaca: tonos cardiacos arrítmicos con soplo eyectivo 3/6 en foco aórtico con irradiación a fosa supraesternal y abolición de segundo ruido. Ingurgitación yugular. Auscultación respiratoria: sibilancias dispersas en ambos campos. Crepitantes en región subescapular derecha y en tercio medio de campo inferior. Semiología de derrame pleural izquierdo. Edemas en ambas extremidades inferiores hasta rodillas.
Pruebas complementarias
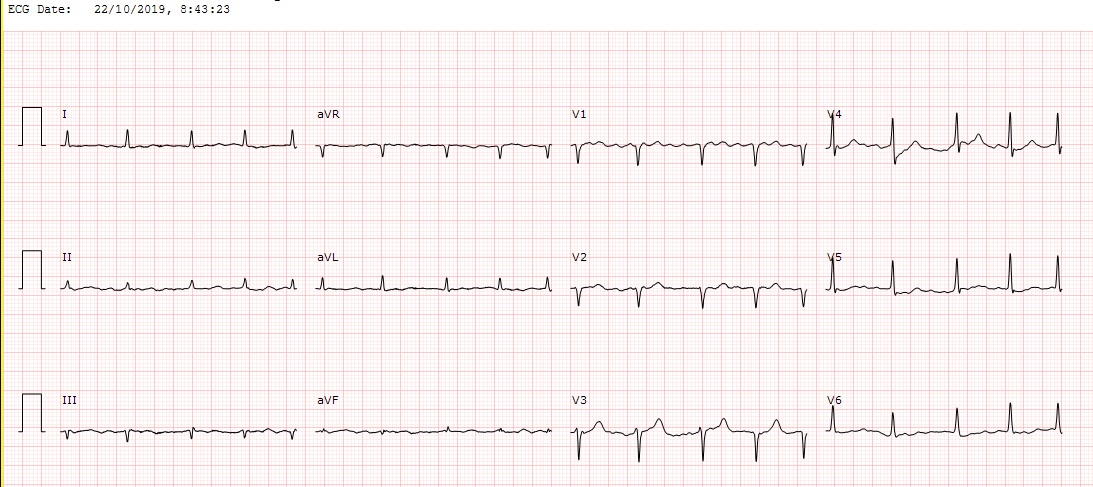
Electrocardiograma (figura 1): fibrilación auricular con frecuencia ventricular media 100 lpm. QRS estrecho. Bajos voltajes en derivaciones del plano frontal. Ausencia de criterios de crecimiento ventricular izquierdo. Escasa progresión de onda R en precordiales. Discreto infradesnivel del segmento ST V3-V4 y onda T aplanada V5-V6.
Analítica: glucosa 140mg/dL, urea 75mg/dL, creatinina 1.22mg/dL (filtrado glomerular: 51mL/min). Ionograma normal. Hemograma normal. Inmunofijación en sangre y orina negativos.
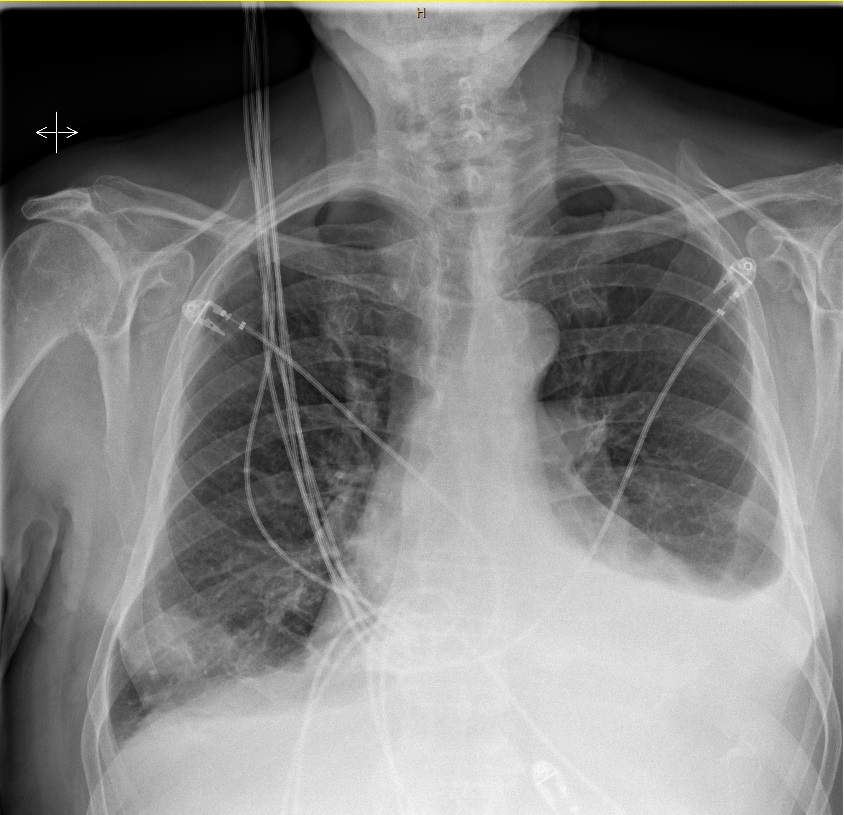
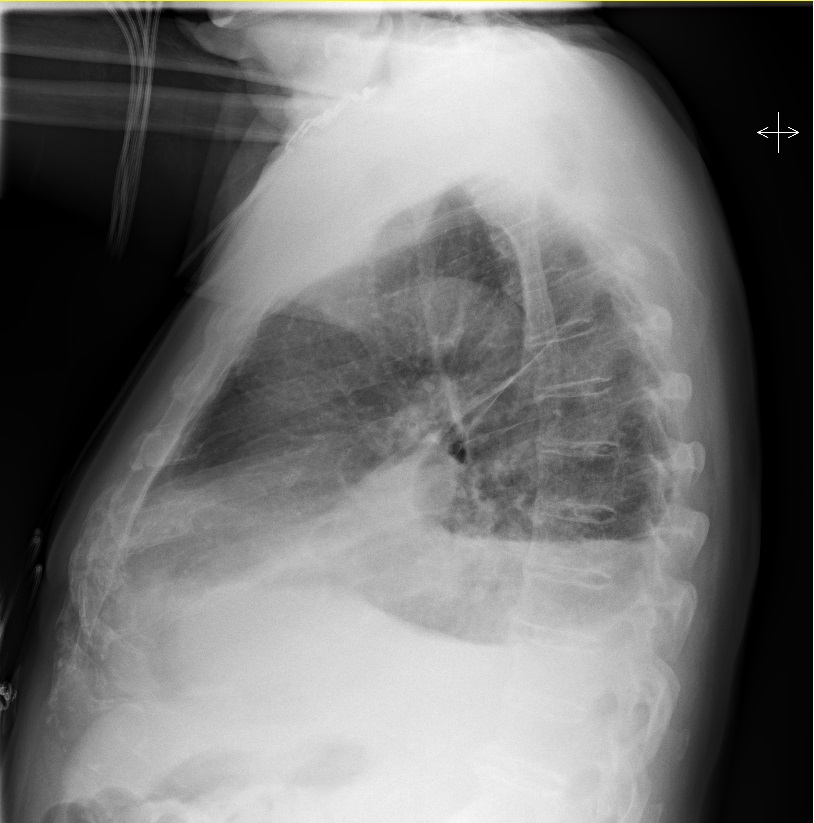
Radiografía tórax (figuras 2A y 2B): imagen compatible con derrame pleural izquierdo.
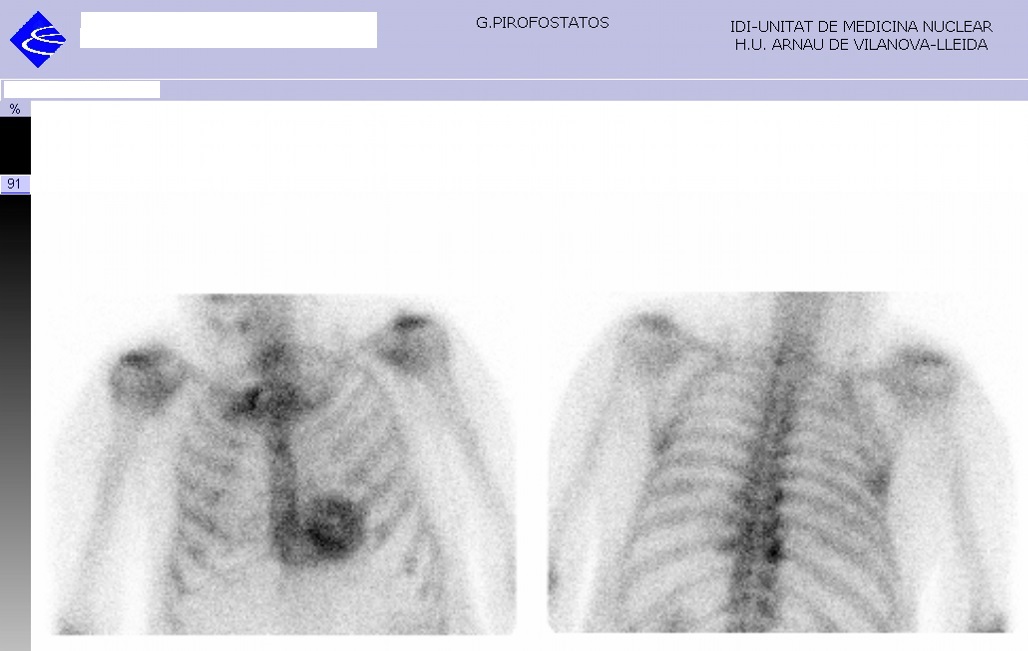
SPECT pirofosfatos (figura 3): se realizan imágenes planares a la región torácica a las dos horas post-administración del radiofármaco donde se observa un intenso deposito del radiofármaco en el miocardio que presenta distribución biventricular. Conclusión: estudio compatible con amiloidosis cardiaca. Grado 2.
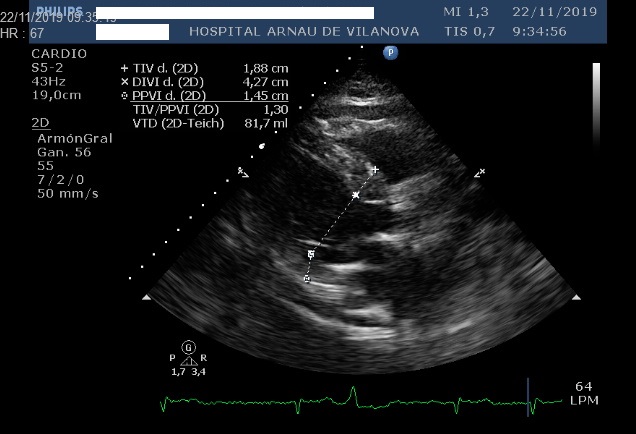
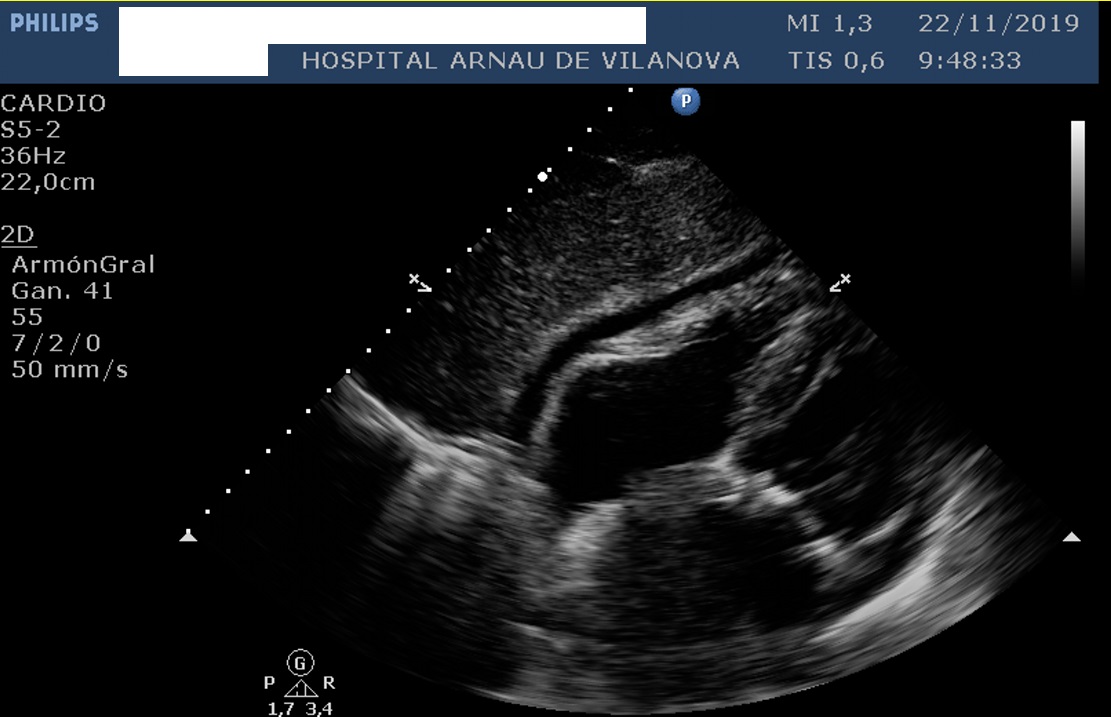
Ecografía cardiaca transtorácica (figuras 4, 5 y 6. Vídeo 1): doble lesión aórtica degenerativa: estenosis severa e insuficiencia ligera. Insuficiencia mitral degenerativa ligera. Ventrículo izquierdo no dilatado, severamente hipertrofiado, con función sistólica normal. Severa dilatación de aurícula izquierda y moderada de la derecha. Hipertensión pulmonar moderada. Derrame pericárdico ligero.
Diagnóstico
- Insuficiencia cardiaca con fracción de eyección preservada.
- Amiloidosis cardiaca por transtirretina wild-type (TTRwt).
- Estenosis aórtica degenerativa severa.
- Fibrilación auricular permanente.
- Enfermedad renal crónica.
- Paciente frágil.
Evolución
El paciente ingreso en la planta de Cardiología iniciándose tratamiento depletivo endovenoso; y con vistas a valorar la indicación de sustitución valvular aórtica percutánea. Sin embargo, al ingreso destacaba en el electrocardiograma pequeños voltajes en derivaciones del plano frontal e imagen de “pseudoinfarto anterior” en paciente con estenosis aórtica severa e hipertrofia ventricular izquierda moderada. Ante estos hallazgos electrocardiográficos se completó el estudio de IC-FEp realizándose una ecografía cardiaca transtorácica, superponible a la previa con derrame pericárdico ligero sin datos de compromiso ecocardiográfico, y gammagrafía con pirofosfatos que evidenció amiloidosis cardiaca por TTR. Con el fin de descartar una amiloidosis AL, se completó el estudio analítico con proteinuria de Bence-Jones e inmunofijación en sangre y orina que fue negativo.
Por lo tanto, ante amiloidosis cardiaca por TTRwt, en un paciente de edad avanzada, frágil (FRAIL: 4 puntos) y en clase funcional III NYHA; dada la futilidad del recambio valvular percutáneo se desestimó para dicha terapia; decidiéndose manejo sintomático con optimización del tratamiento diurético.
Durante el ingreso evoluciono favorablemente desde el punto de vista congestivo, lo que permitió el alta hospitalaria. La frecuencia cardiaca se controló con betabloqueantes a dosis bajas, con buena tolerancia clínica. Hasta el momento actual no ha presentado nuevos episodios de descompensación.
Discusión
La amiloidosis cardiaca es una enfermedad infiltrativa por depósito extracelular de proteínas. De las proteínas proamiloidóticas a nivel cardiaco, la transtirretina (TTR) produce una de las formas más frecuentes, ya sea por mutaciones o en su forma natural (wild-type)1.
No se conoce con exactitud la prevalencia de la amiloidosis TTRwt. Existen datos en la literatura que muestran una prevalencia de depósito de TTR del 25% en autopsias realizadas a personas mayores de 80 años2; y en autopsias de pacientes con IC-FEp, el 5% presentaba depósito de TTR3. En pacientes mayores de 60 años con hipertrofia ventricular izquierda ligera (≥ 12mm) e IC-FEp, se evidenció una prevalencia del 13%4. En cuanto a la edad de presentación, su inicio típico es en mayores de 60 años; y predomina en varones (89-98% según las series).
En cuanto a la presentación clínica depende tanto del depósito de TTR a nivel cardiaco como a nivel extracardíaco.
A nivel cardiaco, el depósito produce engrosamiento de las paredes ventriculares que progresivamente da lugar a disfunción diastólica. La IC es la forma más frecuente de presentación, sin embargo, la sospecha clínica no debe limitarse a pacientes con IC-FEp, ya que a medida que el depósito de amiloide progresa, la función contráctil empeora. Otros “red flags” que nos deben hacer pensar en esta patología son las alteraciones en la conducción cardiaca (debido a la infiltración amiloide del sistema de conducción) y las arritmias auriculares. También es importante destacar la coexistencia de amiloidosis por TTR y estenosis aórtica degenerativa (un estudio mostró una prevalencia de amiloidosis por TTR del 6% entre pacientes mayores de 65 años sometidos a reemplazo valvular aórtico), siendo que los pacientes con ambas patologías muestran un pronóstico posoperatorio peor frente a los que no presentan amiloidosis por TTTR1.
En cuanto a la afectación extracardíaca, las “red flags” que nos deben hacer sospechar esta entidad, son la estenosis del canal lumbar, la rotura atraumática del tendón del bíceps o “signo de Popeye” y el síndrome del túnel carpiano.
Desde el punto de vista de las técnicas diagnósticas, a nivel electrocardiográfico el hallazgo más frecuente es el patrón de pseudoinfarto. Otros hallazgos que nos pueden hacer pensar en esta patología son los bajos voltajes en el electrocardiograma, bloqueo de rama izquierda del haz de His y la fibrilación auricular.
Aunque el ecocardiograma es muy útil en el diagnóstico, ningún hallazgo es específico. Los signos ecocardiográficos clásicos son hipertrofia ventricular izquierda (hasta en un 25% de los casos asimétrica), el aspecto granular o “sparkling” del miocardio, la hipertrofia del ventrículo derecho, dilatación biauricular, derrame pericárdico leve, engrosamiento de las válvulas auriculoventriculares y la disminución del strain longitudinal en los segmentos basales y medios (patrón “ojo de buey”).
La resonancia magnética es una técnica muy útil en la identificación precoz, siendo el patrón subendocárdico global patognomónico de amiloidosis cardiaca, pero solo está presente en el 25% de los pacientes. La gammagrafía cardiaca 99mTc-DPD es de gran utilidad para el diagnóstico, dada su alta sensibilidad y especificidad, y además puede demostrar afectación cardiaca cuando la ecografía y la resonancia magnética cardiaca aún son normales. La captación grado 2-3 junto con la ausencia de componente monoclonal tiene una especificidad y valor predictivo positivo para amiloidosis cardiaca por TTR del 100%.
La mediana de supervivencia en pacientes no tratados oscila de los 2,5 a 3,6 años tras el diagnóstico, y la mortalidad se debe en la mayoría de los casos a IC y/o muerte súbita.
El manejo de esta patología implica dos aspectos: el tratamiento de soporte (manejo IC, de arritmias auriculares y el implante de dispositivos); y el tratamiento específico para intentar detener o retrasar el depósito de amiloide. En los últimos años se han desarrollado diversos fármacos para tratar frenar el curso de la enfermedad; y en este último aspecto destaca el tafamidis, un estabilizador de TTR, ha supuesto un cambio en el paradigma del manejo de esta patología, ya que la evidencia actual muestra un aumento de la supervivencia (reducción de mortalidad por todas las causas y de las hospitalizaciones relacionadas con enfermedad) con una mejor calidad de vida y buen perfil de seguridad5.
En lo referente a nuestro caso, la prevalencia de estenosis aórtica degenerativa y de amiloidosis cardiaca aumenta con la edad, y su asociación no es infrecuente en los ancianos. La identificación de amiloidosis cardiaca es un desafío en los pacientes con estenosis aórtica, porque estas dos patologías comparten una serie de características.
Aproximadamente ≤15% de los pacientes con estenosis aórtica y ≤30% de los pacientes con estenosis aórtica con patrón de bajo flujo y bajo gradiente pueden tener amiloidosis cardiaca. En los pacientes con estenosis aórtica, la amiloidosis se asocia con mayor riesgo de IC, mortalidad y futilidad del reemplazo valvular aórtico. Si se sospecha amiloidosis, es crucial confirmar el diagnóstico para guiar el tratamiento de la estenosis aórtica. Debido al alto riesgo quirúrgico de los pacientes con estenosis aórtica y amiloidosis cardiaca concomitante, el reemplazo de la válvula aórtica transcatéter puede valorarse y ser preferible a la cirugía6.
Imágenes
Vídeo
Bibliografía
- E. González-López et al. Diagnóstico y tratamiento de la amiloidosis cardiaca por transtiretina. Progreso y esperanza. Rev Esp Cardiol. 2017;70(11):991–1004.
- M.S. Maurer, P. Elliott, R. Comenzo, M. Semigran, C. Rapezzi. Addressing common questions encountered in the diagnosis and management of cardiac amyloidosis. Circulation., 135 (2017), pp. 1357-1377.
- S.F. Mohammed, S.A. Mirzoyev, W.D. Edwards, et al. Left ventricular amyloid deposition in patients with heart failure and preserved ejection fraction. JACC Heart Fail., 2 (2014), pp. 113-122.
- E. González-López, M. Gallego-Delgado, G. Guzzo-Merello, et al. Wild-type transthyretin amyloidosis as a cause of heart failure with preserved ejection fraction. Eur Heart J., 36 (2015), pp. 2585-2594.
- Mathew S. Maurer et al. Tafamidis Treatment for Patients with Transthyretin Amyloid Cardiomyopathy. N Engl J Med. 2018 Sep 13; 379(11):1007-1016.
- Ternacle, J et al. Aortic Stenosis and Cardiac Amyloidosis. J Am Coll Cardiol. 2019;74(21):2638-51.
Autores:
Lucía Matute Blanco. Médico Interno Residente 5º año Cardiología. Hospital Universitario Arnau de Vilanova, Lleida.
Jara Gayán Ordas. F.E.A. Cardiología. Hospital Universitario Arnau de Vilanova, Lleida.
Emilia Blanco Ponce. F.E.A. Cardiología. Hospital Universitario Arnau de Vilanova, Lleida.


