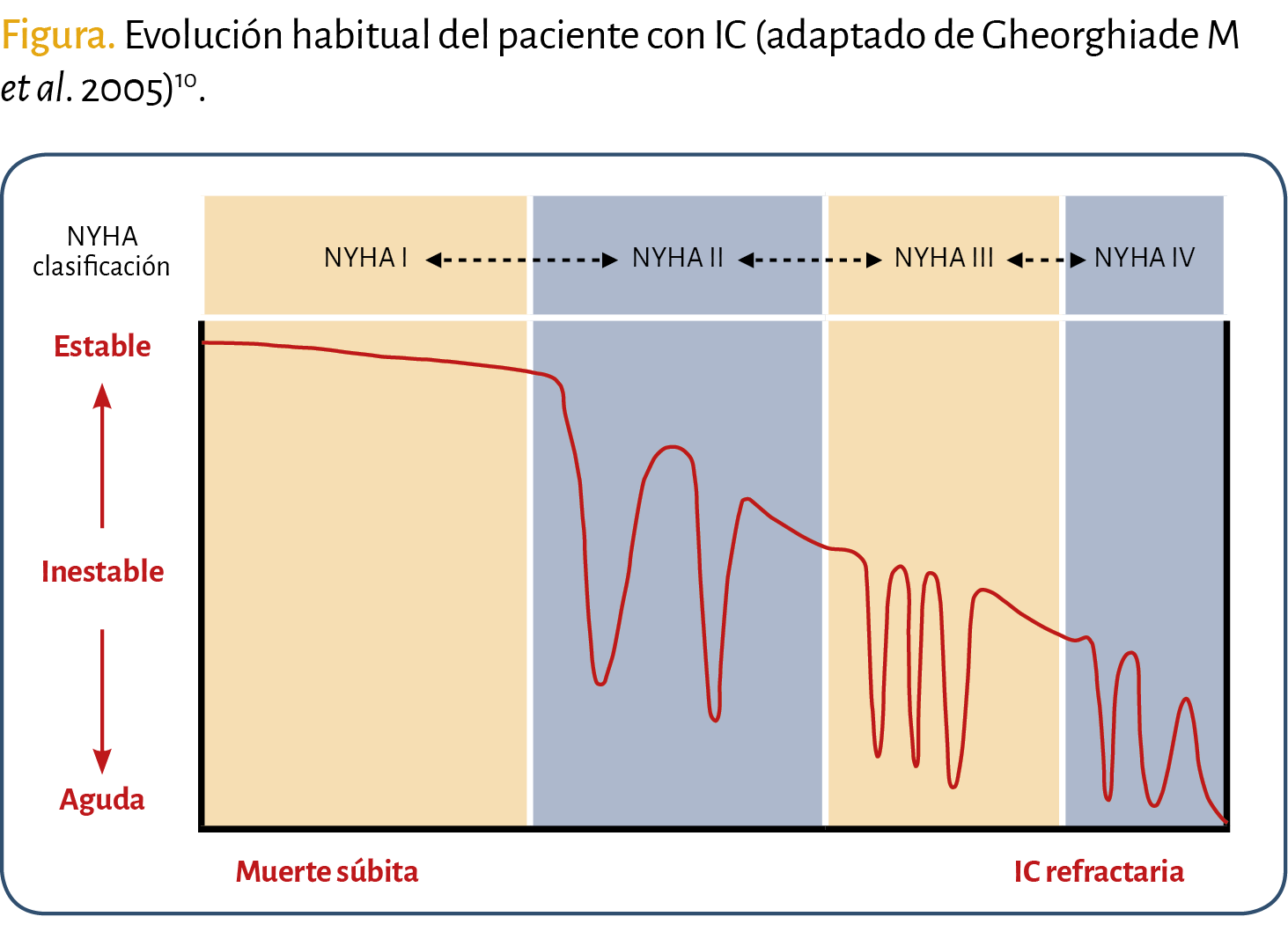
Esta newsletter se podría terminar muy pronto con una respuesta negativa, porque como veremos, el paciente con insuficiencia cardiaca (IC) es un paciente estable hasta que deja de serlo, que suele ser lo habitual (Figura).
Para empezar, vamos a definir la estabilidad del paciente con IC. Las guías NICE1 la definen como aquel paciente que no ha sufrido ingresos hospitalarios ni ajustes en la medicación desde la última revisión ambulatoria. En esta definición se incurre en una contradicción al hablar de la ausencia de ajuste del tratamiento, ya que como veremos, uno de los factores que se asocia con un peor pronóstico en estos pacientes supuestamente estables es la inercia terapéutica, es decir, no optimizar el tratamiento al pensar que el paciente está bien.
Uno de los trabajos iniciales que evaluó el riesgo de estos pacientes con IC “estable” fue este análisis de la población del condado de Olmsted2. Entre estos pacientes, aquellos en el estadio C de la clasificación AHA/ACC (es decir, sintomáticos), se subdividieron en C1 (más estables, sin cumplir criterios de IC de Framingham) y C2 (aquellos con criterios de IC de Framingham). Como podría ser esperable, la mortalidad a los 5 años era mayor en aquellos con más síntomas o signos (estadio C2) a pesar de un tratamiento optimizado (mortalidad a 5 años del 40%), pero en aquellos sin signos o síntomas de Framinghan (estadio C1), la mortalidad a 5 años era del 22%, muy por encima de aquellos pacientes con cardiopatía como disfunción sistólica pero sin IC (estadio B), cuya mortalidad a 5 años era solo del 4%. En este estudio podemos comprobar como la estabilidad no significa baja mortalidad. Más recientemente, un subanálisis del estudio PARADIGM-HF3 nos confirma estos datos. En él evalúan el pronóstico de los pacientes que no habían tenido ningún ingreso previo por IC antes de randomizarse. Hay que recordar que muchos pacientes estaban en clase II y el 37% del total no había tenido ninguna hospitalización previa. Pues bien, en estos pacientes, que eran los más estables, durante el seguimiento medio de 27 meses, el 20% sufrió un evento primario (hospitalización por IC o muerte cardiovascular) y el 17% murió. En el 51% de estos pacientes más estables que murieron durante el estudio, el evento principal fue la muerte CV, y el 60% de esas muertes CV fueron muertes súbitas cardiacas.
Son muchas las causas que confieren este aumento progresivo del riesgo de complicaciones en el paciente con IC aparentemente estable, ya que habitualmente aunque el paciente se encuentra bien, existe una progresión subclínica de la enfermedad. Los principales determinantes de esta progresión son la apoptosis de los cardiomiocitos, el daño mitocondrial, irregularidades en el calcio intracelular, el estrés de pared, la fibrosis miocárdica progresiva y a nivel extracardiaco, la activación neurohormonal4. Todos estos mecanismos provocan un daño miocárdico progresivo, que se manifiesta biológicamente como una elevación de biomarcadores. De hecho, una forma de poder estratificar entre los pacientes teóricamente estables, sería determinar los biomarcadores en su seguimiento, como por ejemplo la troponina o los péptidos natriuréticos. La normalidad de sus niveles y/o la ausencia de elevaciones en el seguimiento se ha relacionado con mejor pronóstico y menor riesgo de hospitalizaciones5,6. En este mismo sentido, entre los pacientes con IC “estable” también tienen un mejor pronóstico aquellos que mejoran o normalizan su fracción de eyección del ventrículo izquierdo en el seguimiento7.
Frecuentemente conseguimos esta falsa estabilidad clínica a base de tratamiento diurético, ya que alivia los síntomas, pero el uso mantenido de diuréticos, también se relaciona con peor pronóstico. Dini FL et al.8 analizaron la importancia de los diuréticos en el paciente aparentemente asintomático y sin congestión, es decir, “estable”. El hecho de que este paciente precise diuréticos para alcanzar dicha situación clínica es un indicador de mayor gravedad y peor pronóstico, reflejando que dicha estabilidad no es real. Además, el uso mantenido de diuréticos se relaciona con un aumento de la morbilidad, especialmente empeoramiento de la función renal e hipotensión, que complica la introducción de nuevos fármacos que realmente sí mejoran el pronóstico (IECA, ARA-II, BB, ARM o INRA).
Directamente relacionado con el punto anterior, uno de los problemas que tienen estos pacientes es lo que nos muestra el registro multicéntrico alemán REFLECT9. Aquellos pacientes más estables y con menor grado funcional son los que tienen menos optimizado su tratamiento, relacionándose con un peor pronóstico. También, el subanálisis del estudio PARADIGM-HF antes comentado3, mostró que, en estos pacientes más estables, respecto a enalapril, el uso de sacubitrilo-valsartán reducía en un 19% el riesgo del evento primario (muerte CV e ingresos por IC) y en un 25% la mortalidad cardiovascular.
Con todo ello, parece que la estabilidad en el paciente con IC no es real, y será de gran importancia la correcta optimización del tratamiento en cualquier estadio de la enfermedad.
Referencias
- NICE GUIDANCE: Chronic heart failure in adults: management https://bit.ly/2nai8Lg.
- Ammar KA et al. Prevalence and Prognostic Signi cance of Heart Failure Stages. Application of the American College of Cardiology/ American Heart Association Heart Failure Staging Criteria in the Community. Circulation 2007;115:1563-70.
- Solomon SD et al. Ef cacy of Sacubitril/Valsartan Relative to a Prior Decompensation: The PARADIGM-HF Trial. JACC Heart Fail. 2016; 4:816-822.
- Sabbah HN. Silent disease progression in clinically stable heart failure. Eur J Heart Fail 2017;19, 469-478.
- Latini R et al. Prognostic value of very low plasma concentrations of troponin T in patients with stable chronic heart failure. Circulation 2007;116:1242-1249.
- Masson S et al. Prognostic value of changes in N-terminal pro-brain natriuretic peptide in Val-HeFT. J Am Coll Cardiol. 2008;52:997-1003.
- Ruiz-Zamora I et al. Incidence and prognosis implications of long term left ventricular reverse remodeling in patients with dilated cardiomyopathy. Int J Cardiol. 2016;203:1114-1121.
- Dini FL et al. Association of furosemide dose with clinical status, left ventricular dysfunction, natriuretic peptides, and outcome in clinically stable patients with chronic systolic heart failure. Congest Hear Fail 2012;18:98-106.
- Böhm M et al. Treatment of heart failure in real-world clinical practice: ndings from the REFLECT-HF registry in patients with NYHA class II symptoms and a reduced ejection fraction. Clin Cardiol 2015:38:200-207.
- Gheorghiade M et al. Pathophysiologic Targets in the Early Phase of Acute Heart Failure Syndromes. Am J Cardiol 2005; 96:11G–17G.





