La fibrilación auricular (FA) puede ser tanto causa como consecuencia de la insuficiencia cardiaca (IC). Son dos patologías muy interconectadas, que comparten también muchos factores predisponentes como la edad, la hipertensión, la cardiopatía isquémica, el síndrome de apneas del sueño, las valvulopatías, etc.1.
La FA por su lado, produce un aumento de la frecuencia cardiaca, un ritmo irregular, la pérdida de contracción auricular y un incremento de la regurgitación mitral, lo cual favorece el desarrollo de una taquimiocardiopatía que puede derivar en IC. Por otro lado, la IC produce un aumento de las presiones de llenado, alteraciones en la regulación del calcio y una activación neurohormonal, que favorece la fibrosis y el aumento de tamaño de las aurículas, lo que facilita la aparición de FA2. Cuando ambas patologías se combinan, tiene un impacto directo en la mortalidad, aumentado entre 2 y 3 veces su riesgo, cuando se compara con cada patología de forma aislada3.
La prevalencia de FA en pacientes con IC aumenta con la edad, como en la población general. Sin embargo, la prevalencia se mantiene estable cuando se analizan pacientes con IC y fracción de eyección (FEVI) conservada, moderadamente deprimida y gravemente deprimida4. Es decir, no por tener peor FEVI, la probabilidad de presentar FA aumenta, cuando la comparamos con otras causas de IC. A pesar de ello, cuando aparece la FA en un paciente con IC, el pronóstico empeora y aumenta el riesgo de mortalidad, independientemente de su FEVI.
En este escenario, parece lógico que empleemos los tratamientos más efectivos disponibles, tanto para la IC como para la FA. De acuerdo a antiguos estudios clínicos (AFFIRM y AF- CHF)5,6, se prefería la estrategia de control de frecuencia a la de control del ritmo, principalmente con el uso de betabloqueantes. Sin embargo, en los últimos años la ablación con catéter de las venas pulmonares se ha mostrado tan efectiva o mejor que los fármacos en conseguir el mantenimiento del ritmo sinusal. En pacientes con IC se tenía cierto recelo a realizar procedimientos de ablación de venas pulmonares, con el argumento de que el papel de las venas pulmonares en este contexto podría tener menos valor, al favorecer la IC la presencia de fibrosis auricular y el aumento de tamaño auricular izquierdo. Sin embargo, en la actualización de las guías de 20197, se introdujo el tratamiento mediante ablación con catéter de las venas pulmonares, en pacientes con IC y FEVI deprimida, como nivel IIb, con el objetivo de reducir la mortalidad y la tasa de hospitalizaciones por IC. Este grado de recomendación es incluso mayor (clase I y IIa, con nivel de evidencia B) en las últimas guías de 2020 de la ESC8. Esto es debido a los resultados de una serie de estudios clínicos realizados en los últimos años. Los estudios iniciales no aleatorizados empezaron a mostrar un aumento de la FEVI tras la ablación de venas pulmonares en pacientes con FA y disfunción ventricular, probablemente secundaria a taquimiocardiopatía9.
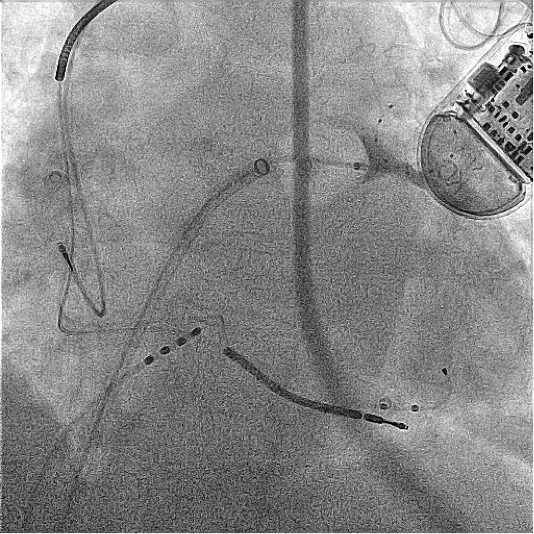
Figura. Crioablación de venas pulmonares en paciente portador de DAI con terapia de resincronización.
Más recientemente se han publicado algunos estudios aleatorizados, con pocos pacientes, pero con resultados muy interesantes10. El estudio CAMERA-MRI11, de 68 pacientes con FA persistente y miocardiopatía dilatada idiopática con FEVI < 45%, pudo demostrar que los pacientes sometidos a ablación tenían menos carga de FA que los que se aleatorizaban a control de frecuencia con fármacos, y eso conllevaba una mejoría significativa de la FEVI en ese grupo (18 ± 13% frente a 4,4 ± 13%). Los pacientes sometidos a ablación conseguían superar el 50% de FEVI en un 58% frente al 9% en el grupo de fármacos, y lo que es más interesante, la mejoría era mucho mayor en los pacientes que no tenían retención de gadolinio en los ventrículos en una resonancia realizada antes de la ablación. Otra conclusión importante fue que la mejoría de la FEVI fue mayor en los pacientes que recuperaban el ritmo sinusal con ablación, incluso al compararse con los pacientes que mantenían un adecuado control de la frecuencia cardiaca en FA, lo que sugiere que, al menos en algunos casos, la FA favorece la miocardiopatía por otros mecanismos que no son únicamente la taquimiocardiopatía.
Por último, el estudio CASTLE-AF12, incluyó a 398 pacientes con FA y miocardiopatía dilatada con FEVI < 35%, monitorizados con desfribrilador automático implantable (DAI) o terapia de resincronización cardiaca (TRC-D) y control remoto, a los que se aleatorizaba entre ablación de venas pulmonares y control del ritmo mediante fármacos. Los pacientes sometidos a ablación, mostraron de forma estadísticamente significativa, una mejor respuesta en el endpoint compuesto de mortalidad y hospitalización por IC, que los pacientes tratados con fármacos. Analizados por subgrupos, los que tuvieron más beneficio fueron pacientes varones, de menos de 65 años, en clase funcional NYHA II y con FEVI > 25%.
En resumen, la coexistencia de FA e IC no es infrecuente y entraña un empeoramiento claro del pronóstico. La ablación de la FA es una técnica segura y eficaz, incluso en algunos pacientes con IC, que conviene tener en cuenta en el armamentarium del tratamiento de esta patología. La individualización en la indicación de la ablación es esencial y podríamos anticipar, según lo anteriormente expuesto, que un candidato idóneo sería aquel con IC, en clase NYHA II, con FEVI > 25%, de menos de 65 años, con una aurícula izquierda no gravemente dilatada y que en una resonancia previa no muestra fibrosis en los ventrículos.
Referencias
- Trulock KM, et al. JACC 2014;64:710-21.
- Anter E, et al. Circulation 2009;119:2516-25.
- Wang TJ, et al. Circulation 2003;107:2920-5.
- Sartipy U, et al. JACC Heart Fail 2017;5:565-74.
- Wyse DG, et al. N Engl J Med 2002;347:1825-33.
- Roy D, et al. N Engl J Med 2008;358:2667-77.
- January CT, et al. Circulation 2019;140:e125-e151.
- 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation. Eur Heart J 2020. (in press).
- Hsu LF, et al. N Engl J Med 2004;351:2373-83.
- Adeliño R, et al. REC CardioClinics 2020. DOI: 10.1016/j.rccl.2020.02.002.
- Prabhu S, et al. JACC 2017; 70: 1949-61.
- Marrouche NF, et al. N Engl J Med 2018;378:417-27.




