Publicado en NEJM
Introducción
La trombina activa las plaquetas a través del receptor PAR-1. Vorapaxar es un nuevo agente antiplaquetario que inhibe selectivamente las acciones celulares de la trombina a través del antagonismo de PAR-1. Este estudio, llamado el TRA 2°P-TIMI 50, fue diseñado para evaluar la eficacia y seguridad de vorapaxar en la reducción de eventos aterotrombóticos en pacientes con aterosclerosis establecida, que estaban recibiendo la terapia estándar.
Material y métodos
Los autores del estudio asignaron aleatoriamente 26449 pacientes que tenían historia previa de infarto de miocardio, accidente cerebrovascular isquémico o enfermedad arterial periférica, a recibir vorapaxar (2,5 mg al día) o placebo y se les siguió durante una mediana de 30 meses. La variable principal de eficacia fue la combinación de muerte por causa cardiovascular, infarto de miocardio o accidente cerebrovascular. Después de 2 años, el comité de seguridad del estudio aconsejó discontinuar el tratamiento en pacientes con antecedentes de accidente cerebrovascular, debido al riesgo de hemorragia intracraneal.
Resultados
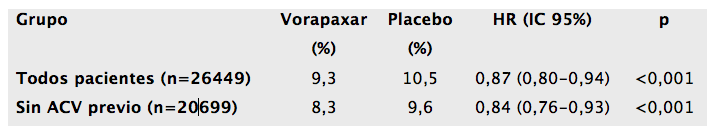
A los 3 años, el objetivo primario ocurrió en 1028 pacientes (9,3%) en el grupo de vorapaxar y en 1176 pacientes (10,5%) en el grupo placebo (razón de riesgo para el grupo vorapaxar, 0,87, 95% intervalo de confianza [IC] , 0,80 a 0,94, P <0,001).

Entre los tres subgrupos de pacientes, este criterio de valoración primario se redujo significativamente en los pacientes post IAM y hubo una pequeña tendencia hacia el beneficio en los pacientes con enfermedad vascular periférica y un efecto neutro en los pacientes con un antecedente de accidente cerebrovascular. La reducción fue significativa tanto en los pacientes que toman y los que no recibieron una tienopiridina al inicio del estudio.
La muerte cardiovascular, infarto de miocardio, ictus o isquemia recurrente que conduce a la revascularización ocurrió en 1259 pacientes (11,2%) en el grupo vorapaxar y 1417 pacientes (12,4%) en el grupo placebo (razón de riesgo 0,88, IC 95%, 0,82 a 0,95 , p = 0,001).
Seguridad
Globalmente, las hemorragias moderadas o graves se presentaron en el 4,2% de los pacientes que recibieron vorapaxar y el 2,5% de los que recibieron placebo (cociente de riesgo = 1,66, IC 95%, 1,43 a 1,93, P <0,001). Hubo un aumento en la tasa de hemorragia intracraneal en el grupo de vorapaxar (1,0% vs 0,5% en el grupo placebo, p <0,001).
Pacientes con accidente cerebrovascular previo

* Criterios TIMI, hemorragia no relacionada con CABG.
Pacientes sin accidente cerebrovascular previo

* Criterios TIMI, hemorragia no relacionada con CABG.
Sangrados moderados-severos (criterios GUSTO) según los distintos subgrupos
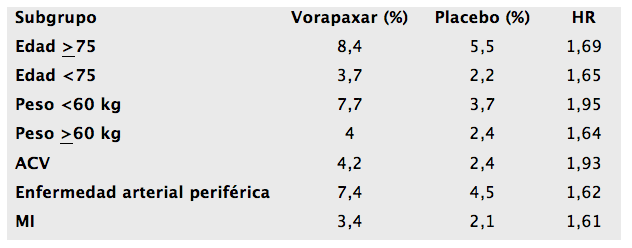
En cuanto a las hemorragias moderadas o graves siguiendo los criterios GUSTO, esta vez se incrementó con vorapaxar en todos los subgrupos de pacientes y fue particularmente problemático en los pacientes con ictus previo y aquellos con un bajo peso corporal.
Conclusiones
La inhibición del receptor PAR-1 con vorapaxar redujo el riesgo de muerte cardiovascular o de eventos isquémicos en pacientes con aterosclerosis estable que estaban recibiendo la terapia estándar. Sin embargo, aumentó el riesgo de hemorragia moderada o severa, incluyendo hemorragia intracraneal.






