Éste es un posible caso a analizar, dentro de la Sección de Imagen Cardiaca.
Varón de 77 años con valvulopatía aórtica degenerativa que acude a urgencias por síndrome febril de evolución subaguda y signos incipientes de insuficiencia cardiaca (2009). Tras extracción de hemocultivos (positivos para S anginosus), se realiza ecocardiograma transtorácico (ETT), que muestra imagen de cavidad pulsátil periaórtica sugestiva de pseudoaneurisma. El ecocardiograma transesofágico (ETE) confirma el diagnóstico de endocarditis complicada por pseudoaneurisma periaórtico que comunica con tracto de salida de ventrículo izquierdo.
Se solicitó una tomografía computarizada (TC) cardiaca y de arterias coronarias para estudio del pseudoaneurisma y su relación con el árbol coronario. El pseudoaneurisma ocupaba una extensión circunferencial de aproximadamente 90º en torno a la raíz aórtica, en la región del seno coronárico izquierdo [figura 1a], caudalmente al origen del tronco común. Se confirmó la presencia de una zona de comunicación con el tracto de salida de ventrículo izquierdo, y se pudo valorar además: a) la puntuación de riesgo de calcio coronario, con un score moderado (130 UH), y b) el estado de las arterias coronarias, que presentaban aterosclerosis difusa pero sin estenosis significativas
Con el diagnóstico de endocarditis aórtica complicada, se procedió a cirugía de recambio valvular aórtico (bioprótesis Magna nº 21), desbridamiento del tejido periaórtico y cierre del pseudoaneurisma residual con parche de teflón. En el control radiológico postquirúrgico persistía imagen de pseudoaneurisma residual excluido con parche [figura 1b], con discreta reducción de su tamaño respecto al estudio realizado previo a la intervención. El paciente completó el tratamiento antibiótico y los hemocultivos al alta fueron negativos.
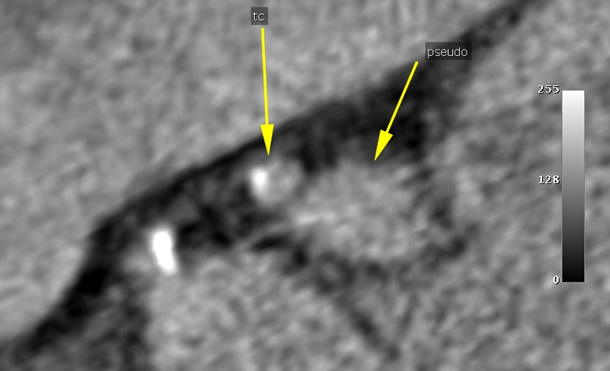
Quince meses más tarde, el paciente ingresó por nuevo síndrome febril de dos semanas de evolución. Se extrajeron hemocultivos (positivos para Streptococo agalactiae) y se realizó un ETT. La prótesis aórtica era normofuncionante, pero mostraba imágenes sugestivas de vegetaciones a nivel de sus discos, así como hiperecogenicidad alrededor del anillo protésico y pseudoaneurisma en zona de interfibrosa mitroaórtica, que protuía hacia aurícula izquierda en sístole [Vídeo 1]. Se realizó ETE para completar el estudio, que confirmó la presencia de dos vegetaciones móviles en el disco correspondiente al seno no coronárico [Vídeo 2], con aparente extensión del absceso en torno al anillo protésico [Figura 2]. Igualmente, se observó una fístula entre pseudoaneurisma, a nivel de la unión mitroaórtica, y tracto de salida de ventrículo izquierdo [Vídeo 3]. Con el diagnóstico de endocarditis activa complicada se planteó tratamiento quirúrgico. Previo a ello, la realización de un TC aportó información de especial relevancia. Por un lado, permitió una mejor delimitación del pseudoaneurisma, que se extendía de forma circunferencial al anillo protésico [Figura 3]. Por otro lado, permitió apreciar la relación del mismo con el árbol coronario: existía un plano de separación entre el pseudoaneurisma y el tronco común, sin evidencia de comunicación entre ambos [Figura 4]. Finalmente, se pudo evaluar el estado de arterias coronarias, que presentaban severa y difusa aterosclerosis, pero sin evidencia de estenosis significativas. Estos datos fueron de gran ayuda para planificar la estrategia quirúrgica, que consistió en explante de la prótesis, desbridamiento amplio de la raíz aórtica, reemplazo con un injerto tubular valvulado y reimplante de las arterias coronarias (Técnica de Bentall).
Discusión
La incidencia actual de endocarditis infecciosa (EI) es predominantemente resultado de patología valvular degenerativa en una población de edad creciente; la mayor prevalencia de pacientes portadores de prótesis valvulares, y su exposición aumentada a infecciones nosocomiales agravan esta tendencia [1]. La enfermedad valvular protésica supone aproximadamente un tercio de todos los casos de EI, y afecta al 1-3% de pacientes sometidos a cirugía valvular cardiaca [2,3]. El diagnóstico se establece mediante los criterios modificados de Duke [4], integrados por factores de riesgo clínicos, resultados microbiológicos y hallazgos ecocardiográficos para estratificar pacientes en tres categorías diagnósitcas (EI definitiva, EI posible, EI improbable). La ecocardiografía representa la piedra angular en su identificación. Sin embargo, la sensibilidad de la ETT es limitada (oscila 18-68%), y suele ser necesario complementar la información con un ETE (sensibilidad y especificidad variables, del 48-100%) [5]. Existen dos situaciones donde las recomendaciones actuales establecen el ETE como técnica de primera elección: diagnóstico de endocarditis valvular protésica y evaluación de complicaciones [7,8]. El paciente presentado cumplía ambas indicaciones.
Una vez establecido el diagnóstico, el seguimiento y orientación terapéutica también guardan un papel para las técnicas de imagen. La mayor aplicación del TC multicorte es la evaluación de la enfermedad arterial coronaria para excluir estenosis >50% [9, 10]. Además, esta técnica se ha demostrado prometedora para la evaluación morfológica y funcional de valvulopatías [11, 12]. Los estudios en endocarditis infecciosa son escasos, pero hay datos que sugieren que la TC podría ser útil para la valoración de dichos pacientes. Al compararlo con ETE, el TC muestra una exactitud diagnóstica similar en la detección de vegetaciones, abscesos o pseudoaneurismas [13]. Nuestro caso añade la posibilidad de seguimiento de dichos pseudoaneurismas y ver su evolución. Si se plantea cirugía, el TC permite: a) evitar una angiografía invasiva, técnica de elevado riesgo en pacientes con vegetaciones sobre válvula/prótesis aórtica (posible embolización); b) Evaluación minuciosa y reconstrucción tridimensional de las relaciones anatómicas de abscesos/pseudoaneurismas perivalvulares con estructuras circundantes. Todo ello facilita la planificación de la intervención.
En conclusión, aunque no existen datos suficientes para realizar un TC como técnica alternativa al ETE, puede complementar la información aportada por éste y describir características de interés para un tratamiento quirúrgico, con frecuencia necesario, y de complejidad técnica importante.
Bibliografía
[1] Bashore TM, Cabell C, Fowler V Jr., et al. Update on infective endocarditis. Curr Probl Cardiol 2006;31:274–352.
[2] Erbel R, Rohmann S, Drexler M, et al. Improved diagnostic value of echocardiography in patients with infective endocarditis by transesophageal approach. A prospective study. Eur Heart J 1988;9:43–53
[3] Sochowski RA, Chan KL. Implication of negative results on a monoplane transesophageal echocardiographic study in patients with suspected infective endocarditis. J Am Coll Cardiol 1993;21:216 –21.
[4] Durack DT, Lukes AS, Bright DK. New criteria for diagnosis of infective endocarditis: utilization of specific echocardiographic finding: Duke Endocarditis Service. Am J Med 1994;96:200–9
[5] Sachev M, Peterson G, Jollis G. Imaging techniques for diagnosis of infective endocarditis. Cardiol Clin 2003;21:185–95.
[6] Erbel R, Rohmann S, Drexler M, et al. Improved diagnostic value of echocardiography in patients with infective endocarditis by transesophageal approach. A prospective study. Eur Heart J 1988;9:43–53.
[7] European Society of Cardiology Task Force Members. Guidelines on Prevention, Diagnosis and Treatment of Infective Endocarditis. Eur Heart J 2009; 30: 2369–2413
[8] ACC/AHA 2006 Guidelines for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2006; 114: 450-527.
[9] Meijboom WB, Mollet NR, Van Mieghem CA, et al. Pre-operative computed tomography coronary angiography to detect significant coronary artery disease in patients referred for cardiac valve surgery. J Am Coll Cardiol 2006;48:1658–65.
[10] Janne d’Othée B, Siebert U, Cury R, Jadvar H, Dunn EJ, Hoffmann U. A systematic review on diagnostic accuracy of CT-based detection of significant coronary artery disease. Eur J Radiol 2008;65:449–61.
[11]Feuchtner GM, Dichtl W, Friedrich GJ, et al. Multislice computed tomography for detection of patients with aortic valve stenosis and quantification of severity. J Am Coll Cardiol 2006;47:1410 –7.
[12] Feuchtner GM, Dichtl W, Schachner T, et al. Diagnostic performance of MDCT for detecting aortic valve regurgitation. Am J Roentgenol 2006;186:1676–81.
[13] Feuchtner GM, Stolzmann P, Dichtl W, Schertler T, Bonatti J, Scheffel H et al. Multislice Computed Tomography in Infective Endocarditis: Comparison WithTransesophageal Echocardiography and Intraoperative Findings. J. Am. Coll. Cardiol. 2009;53;436-444
Material multimedia
Figura 1:
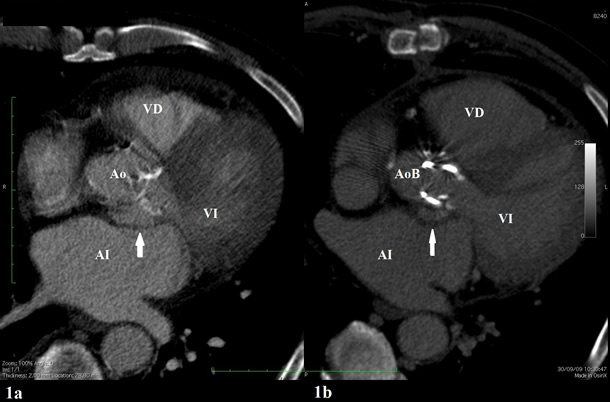
Figura 2
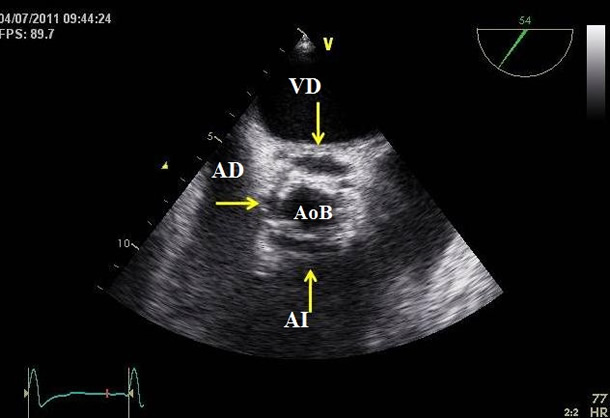
Figura 3
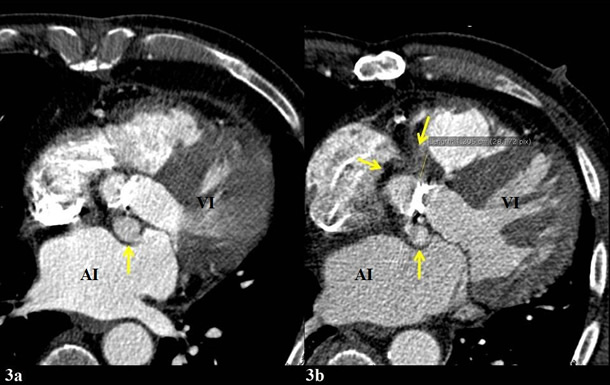
Figura 4
























































![La SEC te lleva a AHA24 [IN] ∙ Estudio SUMMIT](images/telleva/acc24/1.%20SUMMIT.png#joomlaImage://local-images/telleva/acc24/1. SUMMIT.png?width=600&height=336)
![La SEC te lleva a AHA24 [IN] ∙ Estudio BROOKLYN](images/filtros/cardiotv/25.%20BROOKLYN.jpg#joomlaImage://local-images/filtros/cardiotv/25. BROOKLYN.jpg?width=600&height=336)

![La SEC te lleva a AHA24 [IN] ∙ Estudio REALIZE-K](images/filtros/cardiotv/18.%20REALIZE-K.jpg#joomlaImage://local-images/filtros/cardiotv/18. REALIZE-K.jpg?width=600&height=336)
![La SEC te lleva a AHA24 [IN] ∙ Estudio SARAH](images/filtros/cardiotv/20.%20SARAH.jpg#joomlaImage://local-images/filtros/cardiotv/20. SARAH.jpg?width=600&height=336)
![La SEC te lleva a AHA24 [IN] ∙ Estudio CLEAR SYNERGY (OASIS9)](images/filtros/cardiotv/14.%20CLEAR%20OASIS9.jpg#joomlaImage://local-images/filtros/cardiotv/14. CLEAR OASIS9.jpg?width=598&height=336)















.png)


