 La frecuencia cardiaca elevada es un factor de riesgo coronario (1-5) y uno de los principales determinantes de la isquemia y la angina al esfuerzo, por lo que su reducción es una potente arma terapéutica para el tratamiento de los pacientes con cardiopatía isquémica crónica estable. Al arsenal terapéutico clásico de antianginosos bradicardizantes constituido por betabloqueantes, diltiazem y verapamil, se ha sumado en los últimos años Ivabradina.
La frecuencia cardiaca elevada es un factor de riesgo coronario (1-5) y uno de los principales determinantes de la isquemia y la angina al esfuerzo, por lo que su reducción es una potente arma terapéutica para el tratamiento de los pacientes con cardiopatía isquémica crónica estable. Al arsenal terapéutico clásico de antianginosos bradicardizantes constituido por betabloqueantes, diltiazem y verapamil, se ha sumado en los últimos años Ivabradina.
Recientemente se ha aprobado una nueva indicación en asociación a betabloqueantes para el tratamiento de los pacientes con angina y frecuencia cardiaca > 60 latidos por minuto.
El objetivo de este artículo es revisar lo concerniente a la seguridad y tolerabilidad del tratamiento con Ivabradina sola o asociada a betabloqueantes.
¿Es segura la Ivabradina?
Ivabradina es un fármaco seguro y bien tolerado según se desprende de los resultados de los ensayos clínicos fases II y III que han permitido controlar prospectivamente a varios miles de pacientes tratados con Ivabradina. La mayoría de sus escasas reacciones adversas dependen de la dosis (fácil solución) y están relacionadas con su mecanismo de acción (son previsibles).
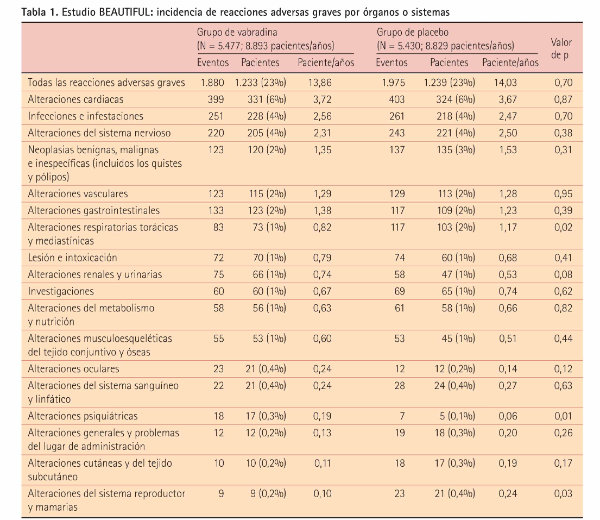
La mayor experiencia controlada para el análisis de la seguridad de Ivabradina procede del estudio BEAUTIFUL (6). En él se trataron con Ivabradina casi 5.500 pacientes con cardiopatía isquémica estable y función ventricular disminuida durante un seguimiento medio de 19 meses. El 87% de los enfermos estaba tratado con betabloqueantes. Las reacciones adversas graves, excluidas las correspondientes a los propios criterios de valoración de efi cacia del estudio, se presentan minuciosamente detalladas según 18 sistemas (tabla 1). Su análisis permite concluir que:
- El número total de complicaciones adversas graves es idéntico en el grupo de Ivabradina que en el grupo placebo.
- En 15 sistemas no se evidencia ninguna diferencia significativa entre las reacciones adversas graves del grupo de Ivabradina respecto al placebo.
- Respecto al grupo placebo, los pacientes que recibieron Ivabradina presentaron menos reacciones adversas graves de tipo respiratorio, torácico o mediastínico (2% vs 1%; p = 0,02) y menos alteraciones del sistema reproductor y mamario (0,4% vs 0,2%; p = 0,03). Por el contrario, los pacientes que recibieron Ivabradina presentaron más alteraciones psiquiátricas (0,1% vs 0,3%; p = 0,01). Aunque significativas, la extraordinariamente baja incidencia
de estas complicaciones no parece preocupante. Probablemente sean producto del azar y no merezcan más que una atención en el seguimiento en
fase IV del producto.
 La reflexión más detallada sobre la seguridad en el uso de la Ivabradina lo merece la aparición de bradicardia excesiva y de alteraciones visuales. Obviamente la bradicardia es el efecto esperado del fármaco. En el estudio BEAUTIFUL, arbitrariamente se consideró que una bradicardia por debajo de 50 latidos por minuto era indicación de suspender el tratamiento, lo que ocurrió en el 13% de los pacientes. Más relevante es la información de que sólo el 2,6% de estas bradicardias fueron realmente sintomáticas y entre ellas, la gran mayoría (112 de 146) ocurrieron en pacientes cuya frecuencia cardiaca basal a la entrada en el estudio era ya ≥ 70 latidos por minuto.
La reflexión más detallada sobre la seguridad en el uso de la Ivabradina lo merece la aparición de bradicardia excesiva y de alteraciones visuales. Obviamente la bradicardia es el efecto esperado del fármaco. En el estudio BEAUTIFUL, arbitrariamente se consideró que una bradicardia por debajo de 50 latidos por minuto era indicación de suspender el tratamiento, lo que ocurrió en el 13% de los pacientes. Más relevante es la información de que sólo el 2,6% de estas bradicardias fueron realmente sintomáticas y entre ellas, la gran mayoría (112 de 146) ocurrieron en pacientes cuya frecuencia cardiaca basal a la entrada en el estudio era ya ≥ 70 latidos por minuto.
Entre los pacientes que al entrar en el estudio presentaban una frecuencia cardiaca en reposo < 70 latidos por minuto sólo hubo 34 casos de bradicardia sintomática (1,3%). Al margen de que esta incidencia pueda interpretarse como alta o baja, lo cierto es que se trata de una complicación no grave y totalmente reversible con la supresión del tratamiento.
En este mismo estudio sólo 37 pacientes (0,3%) tuvieron que dejar el tratamiento por síntomas visuales tales como fosfenos, visión borrosa u otros. Estas alteraciones visuales son producidas por la existencia en la retina de canales de corriente If, similares a los del nodo sinusal (7). Cabe resaltar que estos síntomas dependen de la dosis y aunque en una fase inicial su incidencia puede ser mayor, durante el seguimiento pueden desaparecer hasta en el 80% de las ocasiones. Por tanto, salvo en raras ocasiones y en casos muy severos o especiales (conductores nocturnos o personas sometidas a cambios bruscos de intensidad de luz), no es necesario interrumpir definitivamente el tratamiento, sabiendo que ésto solucionará definitivamente el problema en caso de ser imprescindible.
Otro estudio de gran relevancia para valorar no sólo la eficacia, sino también la seguridad de Ivabradina asociada a betabloqueantes es el estudio ASSOCIATE (8) ya que el 100% de los pacientes tratados con Ivabradina estaban tratados con estos fármacos. En este estudio se incluyeron pacientes con angina ya tratados con dosis media (ej. Atenolol 50 mg) y frecuencia cardiaca > 60 latidos por minuto (frecuencia cardiaca media = 67 latidos por minuto). La dosis de Ivabradina inicial fue de 5 mg c/12 h y si la frecuencia cardiaca a los 2 meses era mayor a 50 latidos por minuto se incrementaba la dosis a 7,5 mg c/12 h. Con este plan se incrementó la dosis de Ivabradina en el 90% de los pacientes betabloqueados, con sólo un 1,1% de abandonos por bradicardia sintomática al fi nal del estudio.
De este estudio se extraen dos conclusiones relevantes. La primera es que la eficacia anti-isquémica de Ivabradina asociada a betabloqueantes se demuestra ya a partir de los 60 latidos por minuto. La segunda es que incluso en pacientes con frecuencia cardiaca relativamente baja, la asociación de Ivabradina a betabloqueantes es segura, con una baja incidencia de bradicardia sintomática.
La eficacia y seguridad de la asociación de Ivabradinaa betabloqueantes en los estudios ASSOCIATE y BEAUTIFUL, han determinado la aprobación definitiva de la EMEA para su utilización conjunta ya a partir de una frecuencia cardiaca de 60 latidos por minuto. Resultados prácticamente idénticos a los hasta aquí comentados se han comunicado con el uso de Ivabradina en pacientes que no estaban tratados con BB, en un reciente metaanálisis (9) que agrupa 5 estudios de angina, el cual además detalla la ausencia de diferencias entre distintos subgrupos de población según edad, sexo u otras patologías asociadas.
¿POR QUÉ IVABRADINA ES SEGURA Y BIEN TOLERADA?
La falta de efectos colaterales, la seguridad y la buena tolerabilidad de Ivabradina a dosis terapéuticas es fruto de dos hechos: la especifi cidad de su lugar de acción y un cierto mecanismo de “autorregulación” o “feedback” negativo que impide aumentar más la bradicardia en corazones con frecuencias cardiacas bajas.
Ivabradina produce un bloqueo selectivo, dependiente de la concentración, de la corriente If de las células del nódulo sinusal (10). Este bloqueo “aplana” la pendiente de despolarización de estas células, que es uno de los principales determinantes del retraso de su despolarización y con ello de la disminución de la frecuencia de descarga de impulsos.
Lo realmente interesante de esta molécula, desde el punto de vista de la seguridad y ausencia de efectos indeseados, es que a concentraciones terapéuticas carece de acción sobre otras corrientes iónicas. Por ello, a diferencia del resto de cronotropos negativos, no modifica ninguna otra propiedad electrofi siológica cardiaca (11) ni ejerce efecto alguno sobre la contractilidad miocárdica ni la presión arterial (12).
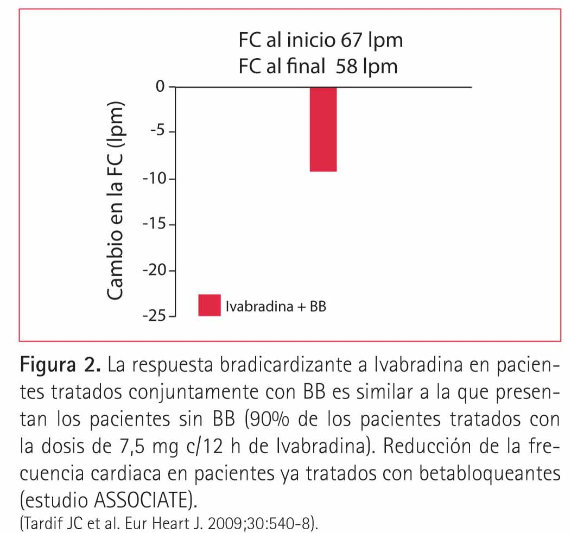
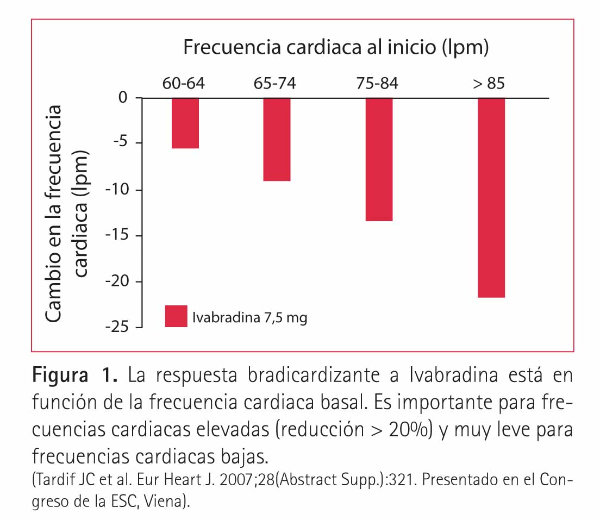 Ivabradina bloquea el canal If desde el interior de la célula. Es decir, para actuar debe penetrar en el citoplasma celular y bloquear el flujo iónico desde la parte interna del canal, lo que implica que el canal If debe estar abierto. Lo más importante es que el grado de bloqueo depende de la frecuencia cardiaca: a mayor frecuencia cardiaca más canales If están abiertos y Ivabradina produce un bloqueo mayor. En cambio a frecuencias cardiacas bajas la cantidad de canales abiertos es menor y se produce un menor bloqueo de los canales por el fármaco. Este hecho tiene una importancia clínica trascendental ya que la reducción de la frecuencia cardiaca será máxima en los pacientes más taquicárdicos mientras que a las dosis terapéuticas se reduce el riesgo de producir bradicardias excesivas (10, 13, 14) (Figura 1). Este mecanismo de acción y respuesta a Ivabradina es independiente de que el paciente esté o no tratado con betabloqueantes (Figura 2). La nueva indicación en ficha técnica apoya esta afirmación, ya que no es necesaria una dosificación diferente de Ivabradina, ni un seguimiento diferente para los pacientes, independientemente de que estén tratados o no con betabloqueantes o de la dosis de éstos que estén recibiendo.
Ivabradina bloquea el canal If desde el interior de la célula. Es decir, para actuar debe penetrar en el citoplasma celular y bloquear el flujo iónico desde la parte interna del canal, lo que implica que el canal If debe estar abierto. Lo más importante es que el grado de bloqueo depende de la frecuencia cardiaca: a mayor frecuencia cardiaca más canales If están abiertos y Ivabradina produce un bloqueo mayor. En cambio a frecuencias cardiacas bajas la cantidad de canales abiertos es menor y se produce un menor bloqueo de los canales por el fármaco. Este hecho tiene una importancia clínica trascendental ya que la reducción de la frecuencia cardiaca será máxima en los pacientes más taquicárdicos mientras que a las dosis terapéuticas se reduce el riesgo de producir bradicardias excesivas (10, 13, 14) (Figura 1). Este mecanismo de acción y respuesta a Ivabradina es independiente de que el paciente esté o no tratado con betabloqueantes (Figura 2). La nueva indicación en ficha técnica apoya esta afirmación, ya que no es necesaria una dosificación diferente de Ivabradina, ni un seguimiento diferente para los pacientes, independientemente de que estén tratados o no con betabloqueantes o de la dosis de éstos que estén recibiendo.
¿QUÉ MÁS HAY QUE SABER DE IVABRADINA PARA AUMENTAR LA SEGURIDAD?
Ivabradina se biotransforma en el hígado a través del citocromo P450 CYP3A4. Por ello se desaconseja su uso en hepatopatías moderadas-severas y debe evitarse la administración conjunta, o tener especial precaución, con los inhibidores potentes o activadores de este citocromo (tabla 2) ya que elevan o disminuyen considerablemente los niveles plasmáticos de Ivabradina. Especial mención requiere la administración conjunta con verapamilo o diltiazem (inhibidores
moderados del CYP3A4).
Se desaconseja la asociación de Ivabradina con fármacos que alarguen el segmento QT (antiarrítmicos del grupo I, amiodarona, sotalol, pentamidina, eritromicina, etc), no porque tenga efectos electrofisiológicos directos sobre la repolarización sino porque la reducción de la frecuencia cardiaca puede exacerbar la prolongación de un segmento ST ya alargado por estos fármacos.
Aunque no se ha descrito que el fármaco tenga efectos tóxicos sobre la retina incluso tras tratamientos prolongados, sí se recomienda administrar con precaución en pacientes con retinitis pigmentosa. No se debe administrar Ivabradina a niños ni adolescentes por no haberse probado sus efectos en los ensayos clínicos, así como a embarazadas y mujeres en periodo de lactancia, ya que hay datos de experimentación animal que apuntan efectos teratogénicos y embriotóxicos.
Finalmente, no se deberá iniciar el tratamiento en pacientes con frecuencia cardiaca ≥ 60 latidos por minuto. La dosis inicial admitida es de 5 mg/12 horas (recomendado 2,5 mg/12 horas en mayores de 75 años). En función de la respuesta clínica y cronotropa, la dosis se ajustará entre 2,5 y 7,5 mg/ 12 horas.
EN CONCLUSIÓN
Los ensayos clínicos realizados con Ivabradina, sola o asociada a betabloqueantes, demuestran un muy buen perfil de seguridad y buena tolerancia a la toma de este fármaco, prácticamente superponible al del placebo. Sólo una baja incidencia de bradicardia sintomática y una aún menor aparición de alteraciones visuales obligan a retirar el tratamiento (con recuperación ad integrum) aproximadamente en el 2% de los pacientes.
Para extremar la seguridad del tratamiento se debe dosifi car adecuadamente y evitar su administración en determinadas poblaciones (hepatopátas, niños, embarazadas, etc.), así como tener precaución o evitar su uso concomitante con inhibidores/inductores del citocromo P450 CYP3A4.
La buena tolerabilidad al tratamiento y la seguridad del mismo está claramente justifi cada por el específico lugar y mecanismo de acción de Ivabradina, que lo convierten en el único fármaco cronodepresor puro, sin otras acciones colaterales cardiovasculares.
BIBLIOGRAFÍA
- Cook S, Togni M, Schaub MC, et al. High heart rate: a cardiovascular risk factor? Eur Heart J. 2006;27:2387–93.
- Hjalmarson A, Gilpin E, Kjekshus J, et al. Infl uenze of heart rate on mortality after acute myocardial infarction. Am J Cardiol. 1990;65: 547-53.
- Fox K, Borer JS, Camm AJ, et al. Resting heart rate in cardiovascular disease. J Am Coll Cardiol. 2007;50:823-30.
- Giannoglou GD, Chatzizisis YS, Zamboulis C, et al. Elevated heart rate and atherosclerosis: An overview of the pathogenetic mechanisms. Int J Cardiol. 2008;126:302-12.
- Heidland UE, Strauer BE. Left ventricular muscle mass and elevated heart rate are associated with coronary plaque disruption. Circulation. 2001;104:1477-82.
- Fox K, Ford I, Steg PG, et al. Ivabradine for patients with stable coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a randomized, doble.blind, placebo-controlled trial. Lancet. 2008;372:807-16.
- Baruscotti M, Bucchi A, DiFrancesco D, et al. Physiology and pharmacology of the cardiac pacemaker (“funny”) current. Pharmacol Ther. 2005;107:59-79.
- Tardif JC, Ponikowski P, Kahan T. Effi cacy of the If current inhibitor ivabradine in patients with chronic stable angina receiving betablocker therapy: a 4-month, randomized, placebo-controlled trial. Eur Heart J. 2009;30:540–8.
- Tendera M, Borer JS, Tardif JC. Effi cacy of If inhibition with ivabradine in different subpopulations with stable angina pectoris. Cardiology. 2009;114:116-25.
- Bucchi A, Baruscotti M, DiFrancesco D. Current-dependent block of rabbit sino-atrial node If channels by ivabradine. J Gen Physiol. 2002;120:1-13.
- Camm J, Chu-Pak L. Electrophysiological effects of a single intravenous administration of ivabradine (S16257) in adult patients with normal baseline electrophysiology. Drugs R&D. 2003;4:83-9.
- Monnet X, Colin P, Ghaleh B, et al. Heart rate reduction during exercise-induced myocardial ischaemia and stunning. Eur Hert J. 2004;25:579-86.
- Bois P, Bescond J, Renaudon B, et al. Mode of action of bradycardic agent, S 16257, on ionic currents of rabbit sinoatrial node cells. Br J Pharmacol. 1996;118:1051-7.
- Borer J. Drug insight: If inhibitors as specifi c heart-rate-reducing agents. Nature Clin Pract Cardiovasc Med. 2004;1:103-9.
























































![La SEC te lleva a AHA24 [IN] ∙ Estudio SUMMIT](images/telleva/acc24/1.%20SUMMIT.png#joomlaImage://local-images/telleva/acc24/1. SUMMIT.png?width=600&height=336)
![La SEC te lleva a AHA24 [IN] ∙ Estudio BROOKLYN](images/filtros/cardiotv/25.%20BROOKLYN.jpg#joomlaImage://local-images/filtros/cardiotv/25. BROOKLYN.jpg?width=600&height=336)

![La SEC te lleva a AHA24 [IN] ∙ Estudio REALIZE-K](images/filtros/cardiotv/18.%20REALIZE-K.jpg#joomlaImage://local-images/filtros/cardiotv/18. REALIZE-K.jpg?width=600&height=336)
![La SEC te lleva a AHA24 [IN] ∙ Estudio SARAH](images/filtros/cardiotv/20.%20SARAH.jpg#joomlaImage://local-images/filtros/cardiotv/20. SARAH.jpg?width=600&height=336)
![La SEC te lleva a AHA24 [IN] ∙ Estudio CLEAR SYNERGY (OASIS9)](images/filtros/cardiotv/14.%20CLEAR%20OASIS9.jpg#joomlaImage://local-images/filtros/cardiotv/14. CLEAR OASIS9.jpg?width=598&height=336)


















.png)
